深圳市細胞治療技術協會公布默賽爾生物(wù)參與制定的(de)“臨床研究用(yòng)人(rén)類血來(lái)源NK細胞質量規範”技術标準
- 發布時(shí)間:2018-06-26
- 浏 覽:3944次
2017年5月(yuè)11日, 由深圳市羅湖區(qū)人(rén)民醫院牽頭,浙江愛易生物醫學科技有限公司等三家公司參與制定的(de)“臨床研究用(yòng)人(rén)類血來(lái)源NK細胞質量規範”,作爲指導性技術文件經主管部門深圳市衛計委推薦、深圳市市場(chǎng)監督管理(lǐ)局相關工作小組討(tǎo)論後,正式被批準立項。
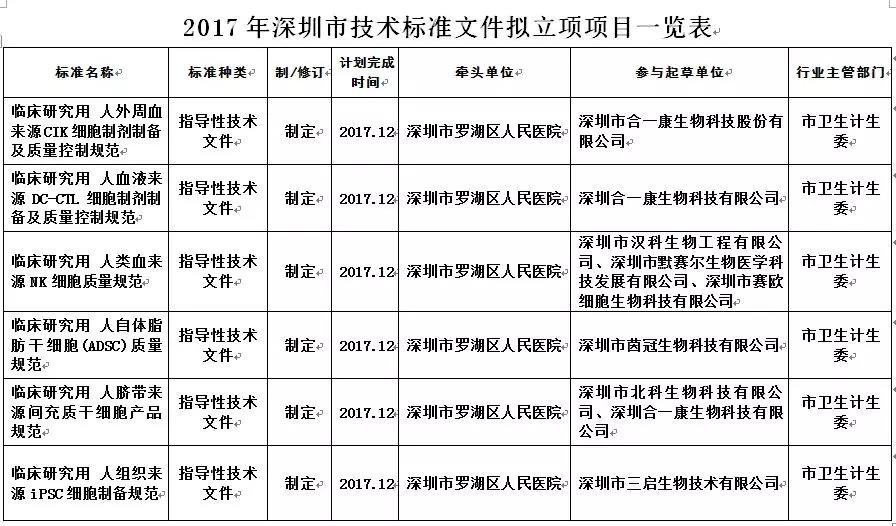
深圳市細胞治療技術協會于2017年9月(yuè)30日,将其中的(de)4項“細胞制劑規範”提交到深圳市标準化(huà)處。2018年6月(yuè)22日,深圳市細胞治療技術協會以團體标準的(de)形式公開其中的(de)4項“細胞制劑規範”,包括默賽爾生物(wù)參與制定的(de)“臨床研究用(yòng)人(rén)類血來(lái)源NK細胞質量規範”(标準編号:SZTT/SSCT 004-2018)。
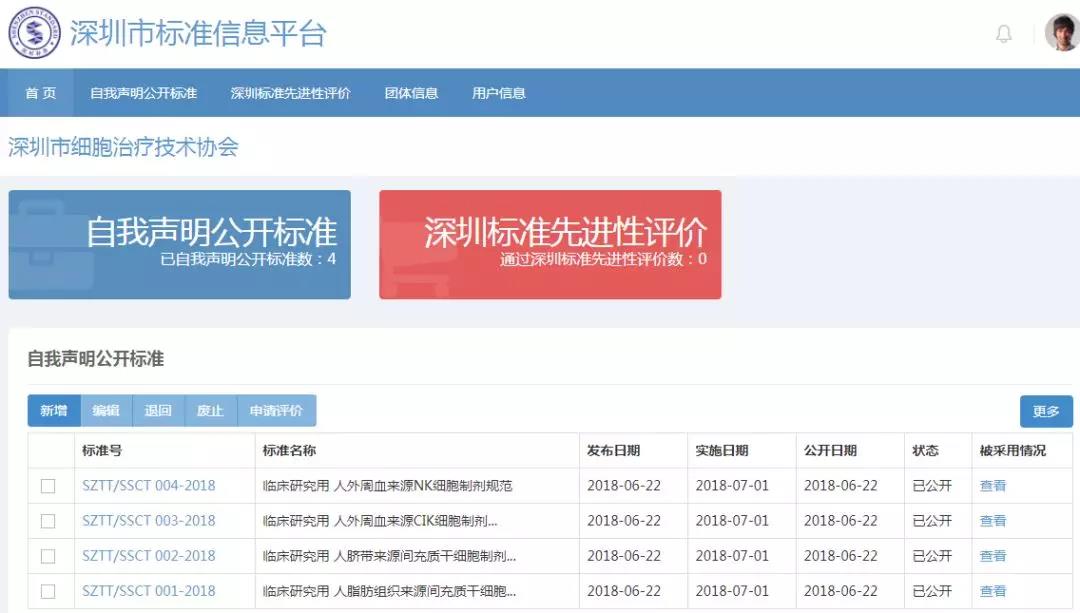
全文獲取方式:
1)登錄深圳市細胞治療技術協會網站http://www.ssctcell.com/點擊“政策法規”欄目查看或點擊下(xià)方“閱讀原文”;
2)登錄深圳市标準信息平台網站http://szbz.sist.org.cn/直接檢索标準名稱。

![二維碼[2021-12-26 16:43:25]
二維碼[2021-12-26 16:43:25]](static/picture/1640508252.jpg)

